Химическая энциклопедия
"НАДУКСУСНАЯ КИСЛОТА"
Главная - Химическая энциклопедия - буква Н - НАДУКСУСНАЯ КИСЛОТА
НАДУКСУСНАЯ КИСЛОТА
(пероксиуксусная
к-та, перук-сусная к-та) СН3С(О)О—ОН, мол.м. 76,05; бесцв. жидкость
с резким запахом; т.пл. — 0,1 °С, т.кип. 110°С, 35-36°С/29мм рт.ст.;
d204 1,1037; nD20
1,3964; DH0обр - 340 кДж/моль (25 °С), DH0исп
44,2 кДж/моль; ур-ние температурной зависимости пара lgp (мм рт.ст.)
= 8,911 — 3211/T; m 7,9.10-30 Кл.м;
хорошо раств. в воде и орг. р-рителях; рКа 8,2 (вода, 20 °С).
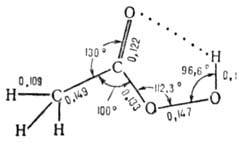
Молекула плоская (длины связей в нм): Н. к. разлагается в парах
до О2, СН3 СООН, СО2, СН3ОН и др.;
энергия диссоциации связи О—О 125-142 кДж/моль. Гидролизуется водными р-рами
щелочей при комнатной т-ре (кат.-переходные металлы, Pt-чернь). Сильный окислитель:
из р-ров иодидов на холоду выделяет I2; окисляет карбонильные соед.
до сложных эфиров; эпоксидирует олефины. Обладает сильным антимикробным, бактерицидным,
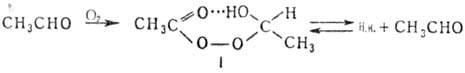
фунгицидным и отбеливающим действием. Получение Н.к.: 1) окислением
ацетальдегида в паровой фазе при недостатке О2 (30% от стехиомстрического)
с добавлением паров ацетона, этилацетата или др. р-рителя либо в жидкой фазе
в среде неокисляющихся орг. р-рителей по схеме: Промежут. аддукт I выделяют
в виде бесцв. кристаллов (т.пл.
20 °С). 2) Кислотно-каталитич.
конденсацией: Н2О2 + СН3СООН Выпускают Н.к. в виде водных
(концентрацией до 40%) и водно-уксусных р-ров, стабилизированных пирофосфатом,
триполифосфатами, тетраметапирофосфатом Na или др. Применяют ее в произ-ве оксидов
пропилена и др. олефинов,
глицерина и капролактама, для отбеливания муки, целлюлозы (бумаги, текстиля),
масел, крахмала и др. Н.к. взрывается при мех.
воздействии (даже в замороженном виде), при нагр. до 100°С. Водные р-ры
концентрацией не менее 50% взрывоопасны. Сильно раздражает слизистые оболочки
глаз и кожу. ЛД50 1410 мг/кг (подкожно, кролики). Лит.: Антоновский
В. Л., Органические перекисные инициаторы, М., 1972, с. 341-61; Swern D., в
кн.: Organic peroxides, v. 1, N.Y.- [а,о.], 1970, p. 313-474. В. Л. Антоновский. |
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: НАДУКСУСНАЯ КИСЛОТА
будет выглядеть так: Что такое НАДУКСУСНАЯ КИСЛОТА
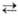
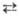 Н.к. +
Н2О. Из реакц. смесей Н.к. выделяют вакуумной перегонкой (давление
не выше 30 мм рт.ст. во избежание взрыва) в присут. стабилизаторов, а также
дробным вымораживанием.
Н.к. +
Н2О. Из реакц. смесей Н.к. выделяют вакуумной перегонкой (давление
не выше 30 мм рт.ст. во избежание взрыва) в присут. стабилизаторов, а также
дробным вымораживанием.