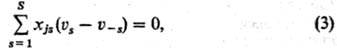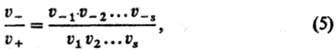Химическая энциклопедия
"СЛОЖНЫЕ РЕАКЦИИ"
Главная - Химическая энциклопедия - буква С - СЛОЖНЫЕ РЕАКЦИИ
СЛОЖНЫЕ РЕАКЦИИ
. Хим.
р-ция реализуется как совокупность множества дискретных актов хим. превращения,
в каждом из к-рых участвует лишь одна или небольшое число частиц (молекул, атомов,
ионов). Если среди актов р-ции имеются химически различающиеся, то р-ция наз.
сложной. К С. р. относят наиб. распространенные классы р-ций-каталитические
(см. Катализ
) и цепные реакции
. Из множества актов С. р.
можно выделить химически одинаковые; они составляют элементарную р-цию. С. р.
представляет собой совокупность элементарных р-ций, природа и последовательность
к-рых составляют механизм реакции
. Всякая элементарная р-ция
в принципе обратима, т.е. всегда наряду с ней возможна р-ция, отличающаяся лишь
направлением превращения (см. Обратимые и необратимые процессы
). Совокупность
элементарной р-ции и обратной ей в составе С.р. наз. стадией С. р. Скорость
u-s обратной р-ции м. б. пренебрежимо мала по сравнению
со скоростью us прямой р-ции, в таком случае s-
ю
стадию считают необратимой. Если, напротив, us = u-s
(или us ! u-s), s-
я
стадия равновесна (квазиравновесна, если us Согласно детального равновесия принципу
, состояние хим. равновесия при С. р. осуществляется
таким образом, что каждая стадия строго равновесна. При удалении реагирующей
системы от равновесия стадии С. р. одна за другой становятся вначале неравновесными,
а затем и необратимыми. Итог С. р. передается одним
или неск. линейно независимыми хим. ур-ниями (стехиометрич. ур-ниями). В-ва,
фигурирующие лишь
в хим. ур-ниях стадий С. р., но не в итоговом ур-нии, наз. промежуточными. Итоговое
хим. ур-ние С. р. может быть получено сложением хим. ур-ний стадий, умноженных
на рациональные числа (положит., отрицат. или равные нулю). Эти числа наз. стехиометрич.
числами С.р. Набор стехиометрич. чисел, обеспечивающий получение итогового ур-ния
(т.е. приводящий к исключению промежут. в-в), задает маршрут р-ции. М.б. образован
базис маршрутов, т.е. такая совокупность маршрутов, что они линейно независимы,
т.е. любой иной маршрут данной р-ции является линейной комбинацией ее базисных
маршрутов. При каждом механизме р-ции число базисных маршрутов определенно,
но выбор их в известной мере произволен. Число базисных маршрутов P больше или равно числу Q независимых итоговых ур-ний. Если P > Q, всегда можно выбрать базис маршрутов таким образом, что итоговым
ур-нием (Р — Q) базисных маршрутов С. р. будет 0 = 0; такие маршруты
наз. пустыми, а базис, состоящий из Q непустых маршрутов и (Р — Q)
пустых,-стехиометрическим. Чтобы определить кинетику
С.р., т.е. представить скорости ее по итоговым ур-ниям в виде ф-ции концентраций
исходных в-в и продуктов, нужно из системы ур-ний, получаемой применением действующих масс закона
к элементарным р-циям, исключить неизвестные концентрации промежут.
в-в. Эта задача упрощается, если р-ция строго стационарна или если ее с достаточным
приближением можно считать квазистационарной: вместо системы дифференц. ур-ний
имеем тогда систему алгебраич. ур-ний, все производные концентрации промежут.
в-в по времени равны нулю (см. Квазистационарности приближение
). С
др. стороны, исследуя нестационарную кинетику, можно получить больше информации
о механизме С. р., чем если ограничиться лишь стационарной кинетикой. Условие стационарности
С. р. записывается в виде: где Система ур-ний, к-рые получаем,
выразив в (1) us и u-s по
закону действующих масс, определяет все неизвестные. Ур-ние (2) позволяет легко
определить число базисных маршрутов данной р-ции. Если к.-л. стадия С. р. равновесна,
ур-ние (1) в применении к этой стадии заменяется ур-нием, выражающим закон действующих
масс для соответствующего равновесия. Для С. р., описываемой неск. итоговыми
ур-ниями, достаточно записать кинетич. ур-ния, выражающие скорости по непустым
маршрутам стехиометрич. базиса (скорости по пустым маршрутам не требуются, хотя
они и не равны нулю). Альтернативное выражение
условий стационарности С. р. имеет вид: где xjs-стехиометрич.
коэф. промежут. в-ва номеру в хим. ур-нии 5-й стадии (положит. число, если в-во
образуется, и отрицательное, если в-во расходуется). Условия (1) и (3) эквивалентны,
иногда удобнее пользоваться одним, иногда-другим. В случае одномаршрутной
С. р. (р-ции с одним базисным маршрутом) ее стационарная скорость u
м.б. выражена через скорости в прямом направлении u+ и в
обратном направлении u_: при этом где u1,
u2, ...-скорости элементарных р-ций всех стадий. Равенство
(5) справедливо независимо от того, каковы стехиометрия, числа стадий. Из него
следует, что если хотя бы одна стадия необратима, то u-=0, т.е.
С.р. в целом необратима. С помощью изотопных индикаторов
можно в ряде
случаев определить отдельно u+ и u- . Если все стадии одномаршрутной
С. р., кроме одной (номер l), равновесны, то равенство (5) дает: u-/u+
! u-l/ul. Тогда,
согласно (4), u+ ! ul,
u-! u-l. Такую стадию
называют скоростьопределяющей или лимитирующей. Если С. р. проходит в условиях,
близких к равновесным, обычно неравновесна лишь одна стадия, она определяет
скорость С. р., если р-ция одномаршрутна. М. И. Темкин. |
Поделитесь с друзьями:
Вы можете поставить ссылку на это слово:
будет выглядеть так: СЛОЖНЫЕ РЕАКЦИИ
будет выглядеть так: Что такое СЛОЖНЫЕ РЕАКЦИИ
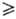 u-s).
По характеру взаимосвязи элементарных р-ций выделяют последовательные р-ции
(продукт предыдущей элементарной р-ции является исходным в-вом последующей),
параллельные р-ции (одновременно протекающие элементарные р-ции, в к-рых по
крайней мере одно из исходных в-в общее), последовательно-параллельные р-ции,
р-ции с циклич. стадиями и т.п.
u-s).
По характеру взаимосвязи элементарных р-ций выделяют последовательные р-ции
(продукт предыдущей элементарной р-ции является исходным в-вом последующей),
параллельные р-ции (одновременно протекающие элементарные р-ции, в к-рых по
крайней мере одно из исходных в-в общее), последовательно-параллельные р-ции,
р-ции с циклич. стадиями и т.п.
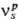 -стехиометрич.
число
-стехиометрич.
число